Este ejercicio tiene un simulador que grafica la neutralización de un ácido con una base y viceversa, tiene controles que permiten modificar la concentración de cualquiera de las dos soluciones y en la gráfica se muestra la variación del pH hasta el punto de neutralización.
Una de las propiedades de las sustancias es su acidez, de acuerdo con esta clasificación las sustancias pueden ser ácidas o básicas. Esta propiedad se basa en la concentración molar de iones hidronio $[H^+]$. Una cantidad muy pequeña de las moléculas de agua se encuentran disociadas en los iones que la forman, los iones hidronio y los iones hidróxido:
$$H_2O\rightleftharpoons H^+ + OH^-$$
Los iones hidronio $[H^+]$ son característicos de las sustancias ácidas y oines hidróxido $[OH^-]$ característicos de las sustancias básicas. El agua pura es neutra por tener ambos iones en igual concentración $[H^+]=[OH^-]=1 \times 10^{-7}mol/l$. El producto $[H^+] [OH^-]=1 \times 10^{-14}mol/l$ siempre se mantiene constante, así que al agregar un ácido, aumenta la concentración de iones hidronio disminuyendo la concentración de iones hidróxido.
La función definida como $p(x)=-log x$ resulta una función muy adecuada para medir la concentración molar de estos iones ya que los valores que se manejan son muy pequeños y el intervalo en el que se trabaja la concentración de iones hidronio es muy amplia $[1,10^{14}]$, se definen entonces las funciones $$pH=-log [H^+]$$ y $$OH=-log [OH^-]$$.
Aplicando las propiedades de los logaritmos a las concentraciones iónicas en el agua se tiene
$[H^+] [OH^-]=1 \times 10^{-14}M$
$p\left([H^+] [OH^-]\right)=p\left(1 \times 10^{-14}\right)$
$-log\left([H^+] [OH^-]\right)=14$
$-log[H^+]-log[OH^-]=14$
$pH+pOH=14$
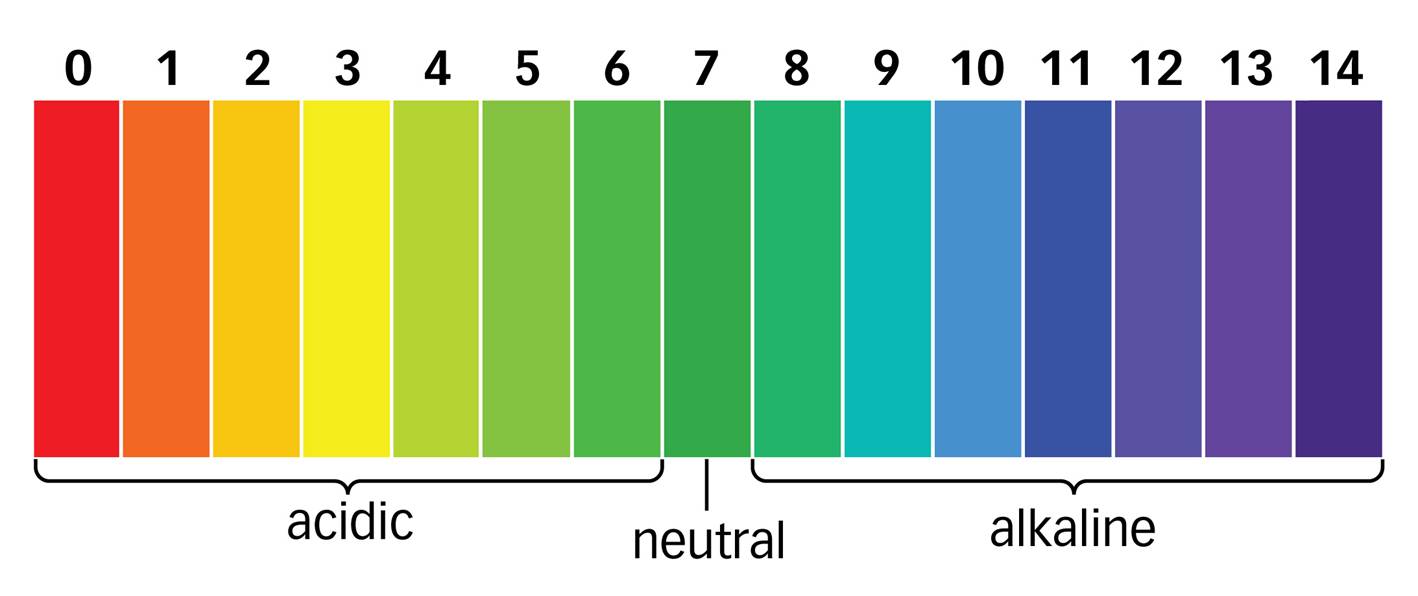
La función pH está definida para valores menores a 7 y la función pOH para los valores mayores de 7, entonces ambas funciones en conjunto pueden definir el intervalo completo de $\[0,14\]$
Titulación ácido base
Una titulación ácido base es un método analítico para determinar el la concentración de una muestra ya sea ácida o básica. Si la sustancia a determinar es un ácido, se agrega gota a gota una solución básica de concentración conocida hasta neutralizar completamente, para determinar el punto final se agrega un indicador, sustancia que toma diferente coloración para sustancias ácidas y básicas. Cada gota de solución básica agregada a la solución problema aumenta ligeramente el pH hasta que logra alcanzar el punto de equivalencia, punto donde se ha neutralizado la solución. En este momento el pH de la solución se eleva rápidamente y el indicador cambia de color. Observa la curva de titulación
Si se continúa agregando solución básica, el pH se mantendrá en valores cada vez más cercano a 14.
La titulación también puede hacerse en sentido inverso, comenzando con una sustancia problema básica y agregar gota a gota una
solución ácida de concentración conocida.